-
Project IDT2021-152
-
受領年2021
-
投資金額¥83,858,773病気Malaria対象Drug開発段階Target Identificationパートナーファイメクス株式会社 , タイ国立遺伝子生命工学研究センター
イントロダクション/背景
1. イントロダクション
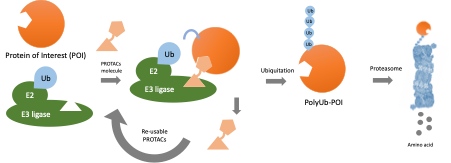
マラリアは、世界中で年間2億人以上が感染している感染症である。しかしながら、既存の抗マラリア薬は、薬剤耐性が問題となっている。薬剤耐性の解決策のひとつとして、新規の作用メカニズムを有する薬剤の開発が考えらえる。近年、PROteolysis-TArgeting Chimeras(PROTAC®)として有名な標的タンパク質分解誘導剤が新規モダリティとして注目されている。標的タンパク質分解誘導剤は、標的タンパク質と結合するwarheadとE3ユビキチンリガーゼに結合する分子をリンカーによって連結した構造を有し、E3ユビキチンリガーゼを標的タンパク質近傍にリクルートすることで、標的タンパク質のユビキチン化を進行させ、ユビキチン化されたタンパク質はプロテアソームによって分解を受ける。しかしながら、マラリア原虫のユビキチンE3リガーゼを用いた標的タンパク質分解誘導剤は報告されていない。これを同定し、使用することができれば、薬剤耐性マラリアに対する画期的な薬剤の創出につながる。
2. プロジェクトの目的
抗マラリアタンパク質分解誘導剤を設計するためのプラットフォームの構築を志向して、マラリア原虫の標的タンパク質を分解するマラリア原虫特有のE3ユビキチンリガーゼをリクルートするE3バインダーを同定する。
3. プロジェクト・デザイン
標的タンパク質の分解実験に供する標的タンパク質分解誘導剤のライブラリーをデザイン・合成する。化合物は、様々なユビキチンE3リガーゼに対するリガンドとマラリア寄生虫のタンパク質として知られているbifunctional dihydrofolate reductase-thymidylate synthaseに特異的に結合するwarheadからデザインする。標的タンパク質の分解が確認された化合物を用いて、後続化合物もデザインする。
本プロジェクトによって、グローバルヘルスの課題はどのように解決されますか?
薬剤耐性を持つマラリア原虫の進化や普及により、マラリアが再燃することが懸念されている。この脅威に対抗する為には、新しい作用機序の新薬が必要である。既存の薬剤が効かないステージを含め、寄生虫のライフサイクルのすべてのステージに作用する薬剤を創出する必要があり、標的タンパク質分解誘導剤はこれらのニーズを満たすことが可能である。標的タンパク質分解誘導剤のアプローチが抗マラリア薬で実証されれば、同じアプローチをリーシュマニア症などの他の寄生虫由来の顧みられない熱帯病への適用が期待される。
本プロジェクトが革新的である点は何ですか?
寄生虫のタンパク質を分解して作用する標的タンパク質分解誘導剤のプラットフォームを確立される。これによりマラリアを始めとする寄生虫由来の疾患を対象とした薬剤の開発に大きく貢献できる。
各パートナーの役割と責任
ファイメクス社(日本)がタンパク質分解誘導剤を合成し、ADME profileの初期スクリーニングを実施する。BIOTEC Institute(タイ)は、タンパク質分解実験と標的タンパク質分解誘導剤の最適化を実施する。
他(参考文献、引用文献など)
最終報告書
1.プロジェクトの目的
PROTACはユビキチンプロテアソーム系UPSを利用し標的タンパク質の分解を誘導する薬剤である。従来の薬剤とは違い標的への強い結合能を必要としないため、創薬標的を広げ、耐性も回避できる。抗マラリアPROTACを開発すべく、マラリア原虫のUPSによる標的分解を誘導する低分子を同定することを目的とする。
2.プロジェクト・デザイン
マラリア原虫の標的酵素に結合する分子にUPSをリクルートする分子を結合させたPROTACを合成し、分解活性を評価した。得られたリード化合物を用いUPSをリクルートするタンパク質同定の検討を行った。また、UPSリクルートリガンドをリンカーで結合したホモ二価化合物を合成し、抗マラリア活性を測定した。
3.プロジェクトの結果及び考察
プロジェクトの成功には、リソースと専門知識を補完し合うパートナーの協力体制が必要である。日本のパートナーであるファイメクス株式会社は、PROTAC探索に関わる高い専門性を活用して、ヘテロ二官能性化合物を設計・合成し、これらの化合物の薬物代謝・薬物動態(DMPK)プロファイルの試験を実施した。海外パートナーであるBIOTECは、抗マラリア薬研究の経験を生かし、化合物の設計・合成、生物学的活性の評価試験を行った。マラリア原虫におけるUPSシステムの誘導に関する知見が限られていた中、迅速な標的分解誘導活性(4時間で50%以上減少)と、強力な抗マラリア活性(50%増殖阻害濃度1μM以下)を示す、UPSリクルートリガンドを結合させた化合物を複数同定した。これらの化合物を医薬品として開発するためには、その作用機序、特に利用されるUPSの構成要素について理解することが不可欠である。光活性プローブを用いて作用機序を解明しようとした最初の試みは、非特異的なタンパク質相互作用のために失敗に終わったが、共免疫沈降法を用いることで、NOT4 E3リガーゼを候補UPS因子として同定することができた。さらに、E3リガーゼリガンドのホモ二価化合物は、リード化合物のヘテロ二価化合物に匹敵する抗マラリア活性を有していた。このことは、NOT4タンパク質そのものが、抗マラリア薬開発におけるPROTACの標的となりうることを示唆している。さらに、ホモ二価化合物は、高い溶解性と代謝安定性を有する良好なDMPKプロファイルを示した。このプロジェクトで得られた有望な結果は、PROTACベースの抗マラリア薬開発へのさらなる投資の価値を示すものである。今後の課題は、さらなる作用機序の検証を行い、二官能性分子がどのようにマラリア原虫のUPSに関与して標的を分解するのかについて包括的に理解することである。
Investment
プロジェクト
PROTACプラットフォームを志向したマラリア由来E3リガーゼの同定と検証




